Revista de la Sociedad Venezolana de Microbiología
versión impresa ISSN 1315-2556
Rev. Soc. Ven. Microbiol. v.29 n.2 Caracas dic. 2009
Betalactamasas tipo AmpC: Generalidades y métodos para detección fenotípica
Dianny Del Valle Martínez Rojas*
Laboratorio de Bacteriología. Servicio Autónomo Hospital Universitario Antonio Patricio de Alcalá. Departamento de Bioanálisis. Universidad de Oriente. Núcleo de Sucre. Venezuela.
Resumen:
Las AmpC son serin-betalactamasas pertenecientes al grupo 1 de la clasificación de Bush-Jacoby-Medeiros, presentes de forma natural en diversas enterobacterias y en bacilos gramnegativos no fermentadores como Pseudomonas aeruginosa y Acinetobacter baumannii. Estas enzimas son capaces de resistir la inhibición por ácido clavulánico, sulbactam y tazobactam. Aunque para la detección de AmpC no existen métodos estandarizados por el CLSI, se han diseñado diversas técnicas con elevada sensibilidad y especificidad. Las betalactamasas AmpC están asociadas a elevada mortalidad y, a nivel de laboratorio, con falsos reportes de susceptibilidad antimicrobiana. Por lo tanto, es de vital importancia su investigación de rutina en los laboratorios de microbiología. En la presente revisión se describe el contexto de las betalactamasas AmpC y algunos métodos disponibles para su detección fenotípica.
Palabras clave: betalactamasas AmpC, resistencia bacteriana, detección fenotípica
AmpC type betalactamases: Generalities and phenotype detection methods
Abstract:
AmpCs are serine-betalactamases belonging to group I of the Bush-Jacoby-Medeiros classification that occur naturally in diverse enterobacteria and non-fermenting gram negative bacilli such as Pseudomonas aeruginosa and Acinetobacter baumannii. These enzymes are capable of resisting clavulonic acid, sulbactam and tazobactam inhibition. Even though there are no standardized methods for detecting AmpC by CLSI, various techniques with high sensitivity and specificity have been designed. AmpC betalactamases are associated with high mortality and, at a laboratory level, with false antimicrobial susceptibility reports. Therefore, its routine investigation is vitally important in microbiology laboratories. In the present review we describe the AmpC context and some methods available for their phenotype detection.
Keywords: AmpC betalactamase, bacterial resistance, phenotype detection
Recibido 9 de enero de 2009; aceptado 21 de octubre de 2009
Introducción
La producción de enzimas constituye el principal mecanismo de resistencia a los betalactámicos en bacterias gramnegativas [1, 2]. A partir de la detección en 1983 de aislamientos clínicos de Klebsiella pneumoniae y Escherichia coli resistentes a cefalosporinas de 3ra generación que, posteriormente, resultaron ser productores de betalactamasas de espectro extendido (BLEE), ha sido significativo el avance en cuanto a la caracterización de estas enzimas [3]. Las AmpC constituyen otro tipo de betalactamasas que, a diferencia de las BLEE, no poseen en la actualidad un método estandarizado por el Instituto de Estándares de Laboratorios Clínicos (CLSI), para su detección fenotípica. Este hecho, aunado a la dificultad para dilucidar fenotípicamente si se está en presencia de una AmpC cromosómica o plasmídica, y a la carencia de inhibidores de AmpC para uso in vivo, hacen considerar a estas enzimas como un emergente problema terapéutico [4]. En el presente artículo se recopilan una serie de métodos, propuestos y probados por diversos investigadores, para la detección fenotípica de betalactamasas tipo AmpC en laboratorios clínicos bacteriológicos. Se pretende además sensibilizar sobre la importancia de identificar y detectar la presencia de AmpC, principalmente las plasmídicas, por su capacidad de transmisibilidad.
Definición y clasificación
Las AmpC son serin-betalactamasas pertenecientes al grupo 1 según la clasificación de Bush-Jacoby-Medeiros [5, 6]. Son también llamadas cefalosporinasas aunque su espectro de acción hidrolítica no sólo incluya cefalosporinas, según se verá más adelante [3, 7]. Ciertas enterobacterias poseen de manera natural betalactamasas tipo AmpC, tal es el caso de Enterobacter spp., Providencia spp., Morganella morganii, Serratia marcescens, Citrobacter freundii y Hafnia alvei [1, 8]; al igual que bacilos gramnegativos no fermentadores de importancia clínica como Pseudomonas aeruginosa [9]. Las AmpC producidas por los microorganismos antes mencionados, son de naturaleza cromosómica inducible y explican la resistencia natural a las aminopenicilinas, cefalosporinas de 1ra generación, cefamicinas (cefoxitina, cefotetán) y aminopenicilinas combinadas con inhibidores de betalactamasas (amoxicilina-ácido clavulánico, ampicilina-sulbactam), expresada por estos agentes bacterianos [1, 8]. E. coli, Shigella spp. y Acinetobacter baumannii, también poseen betalactamasas AmpC cromosómicas pero constitutivas (no inducibles) [1,9,10]. Por otra parte, existen AmpC de codificación plasmídica que pueden ser inducibles o no [11]. Una característica de las enzimas AmpC es que no tienen efecto, por si solas, sobre cefalosporinas de 4ta generación, ni sobre carbapenémicos, siendo estos últimos los betalactámicos de elección en cepas productoras de AmpC [12, 13]. Por otra parte, las AmpC no son inhibidas por los clásicos inhibidores de betalactamasas (ácido clavulánico, sulbactam, tazobactam) [14], aunque algunas pueden ser inhibidas por sulbactam o tazobactam [15, 16].
Sistema de expresión y represión del gen ampC
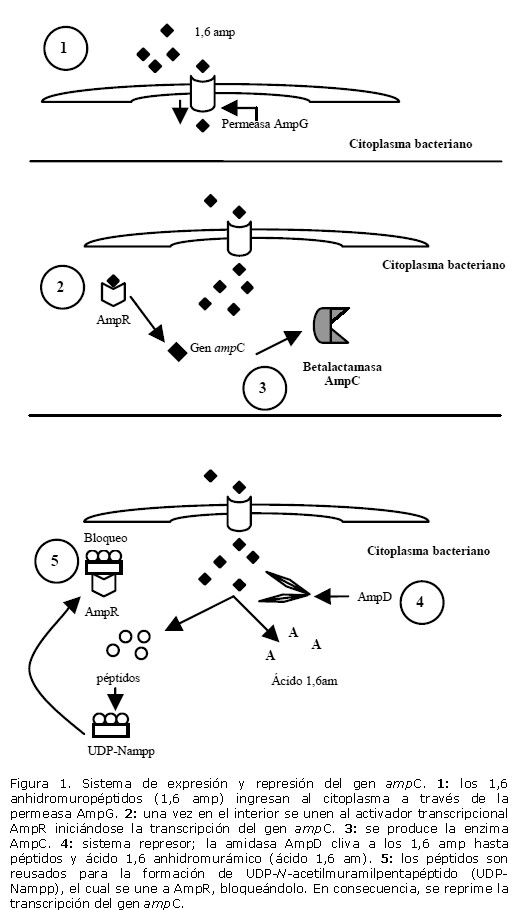
Para comprender la diferencia entre betalactamasas AmpC inducibles y constitutivas, es necesario conocer el mecanismo de expresión y represión del gen que codifica a estas enzimas (gen ampC). Las bacterias que poseen el gen ampC, tienen un complejo sistema molecular regulador de la expresión del mismo, el cual está íntimamente relacionado con el reciclaje del péptidoglicano. El proceso se inicia cuando los productos de degradación de la pared 1,6 anhidromuropéptidos (1,6 amp), ingresan al citoplasma bacteriano a través de una permeasa transmembrana denominada AmpG (codificada por el gen ampG). Estos productos de degradación 1,6 amp, actúan como molécula señal (promotores o inductores) del activador transcripcional AmpR (codificado por el gen ampR). Cuando el AmpR se une a los 1,6 amp se induce la expresión del gen ampC y de esta manera, se produce la enzima AmpC, la cual ejercerá su efecto hidrolítico sobre los betalactámicos para los cuales tiene acción. El sistema represor consiste en el clivaje de los 1,6 amp por la enzima AmpD, la cual es una amidasa citoplasmática (N- acetil-anhidromuramil-l-alaninamidasa) codificada por el gen ampD, hasta ácido 1,6 anhidromurámico y péptidos. Los péptidos son procesados hasta tripéptidos los cuales son reusados resultando en la formación del precursor de la pared celular UDP-N-acetilmuramilpentapéptido. Este, al unirse con el activador transcripcional AmpR, lo bloquea, reprimiendo así la transcripción del gen ampC. Otro gen involucrado es el ampE, el cual, en conjunto con ampD, forma el operón ampDE que codifica una proteína de membrana la cual se piensa actúa como molécula sensora requerida para la inducción [7, 8, 11, 14] (Fig.1). Los betalactámicos inducen la producción de AmpC causando un incremento en la concentración citoplasmática de los productos de degradación 1,6 amp [14]. Todos los betalactámicos son inductores de estas enzimas en mayor o menor grado [1]. Las cepas salvajes productoras de AmpC, lo hacen a bajos niveles (o niveles basales), gracias al sistema represor, por consiguiente, mutaciones asociadas a los genes ampR y ampD, resultan en la hiperproducción de AmpC, un término que se ha denominado derrepresión [11]. En Enterobacter cloacae se ha calculado que uno de cada 105 a 107 aislamientos tendrá la mutación [17], las cuales se producen después de la exposición a betalactámicos. La derrepresión puede ser parcial o total. Los mutantes parcialmente derreprimidos expresan un incremento moderado de los niveles de AmpC; mientras que los mutantes totalmente derreprimidos, expresan altos niveles; por lo tanto, cepas con AmpC natural cromosómica inducible pierden el fenotipo de inducción y pasan a producirla constitutivamente [18].
Las cepas derreprimidas o hiperproductoras, presentan resistencia a todas las penicilinas, combinaciones con inhibidores de betalactamasas, cefalosporinas de 1ra, 2da y 3ra generación, cefamicinas y monobactámicos. Únicamente no se ven afectadas las cefalosporinas de 4ta generación y carbapenémicos, a menos que los microorganismos posean, de forma concomitante, otros mecanismos de resistencia como: pérdida de porinas, BLEE, carbapenemasas entre otros [8].
Clasificación de las betalactamasas AmpC según localización y expresión del gen ampC
AmpC cromosómicas inducibles: Se producen a bajos niveles de manera natural y aumentan su síntesis en presencia de inductores (betalactámicos). Como se mencionó anteriormente, pueden derreprimirse, perdiendo así la característica de inducción. Son ejemplos de bacterias productoras: Enterobacter spp., M. morganii, Providencia spp. P. aeruginosa, entre otras. [1, 9].
AmpC cromosómicas no inducibles (constitutivas): Su expresión es a niveles muy bajos sin mostrar resistencia. Cuando se encuentran hiperproducidas pueden conferir resistencia a todos los betalactámicos a excepción de cefalosporinas de 4ta generación y carbapenémicos. La bacteria representativa es E. coli. [1].
AmpC plasmídicas inducibles y AmpC plasmídicas constitutivas: La evidencia molecular sugiere que los genes que codifican a estas enzimas, derivan de los genes ampC cromosómicos que naturalmente poseen las enterobacterias arriba mencionadas. Estos genes han sido integrados en elementos genéticos transferibles facilitando la diseminación a diferentes microorganismos [19]. Los genes ampC mediados por plásmidos han sido encontrados en bacterias como Salmonella spp., K. pneumoniae y Proteus mirabilis que naturalmente no poseen estos genes [11, 13]. Hasta el presente se han descrito más de 20 familias de AmpC plasmídicas entre las cuales se destacan: ACC, FOX, MOX (incluyen tipo CMY), DHA, CIT y EBC [20]. De estas, 5 son de expresión inducible: DHA-1, DHA-2, ACT-1, CMY-13 y CFE-1 [11]. Al igual que las betalactamasas AmpC cromosómicas hiperproducidas, las enzimas AmpC plasmídicas confieren resistencia a un amplio espectro de betalactámicos incluyendo penicilinas, oxyminocefalosporinas, cefamicinas y, de manera variable, al aztreonam. La AmpC plasmídica tipo ACC-1 representa una excepción debido a que no confiere resistencia a cefamicinas [21, 22]. Se ha determinado que el nivel de expresión de ciertas AmpC plásmidicas inducibles es mucho mayor en comparación con las AmpC cromosómicas inducibles; como ejemplo, la AmpC plasmídica inducible ACT-1 tiene un nivel de expresión de 33 a 95 veces mayor que el de la AmpC cromosómica inducible de E. cloacae. Esto es debido, en parte, al mayor número de copias de genes codificantes de ACT-1 [23]. Es de hacer notar que las AmpC plasmídicas han sido detectadas tanto en aislados intrahospitalarios como en comunitarios [21]. Pai y col. demostraron una alta tasa de fracaso terapéutico en pacientes con septicemia por cepas de K. pneumoniae productoras de AmpC plasmídica tipos DHA-1 o CMY-1, quienes recibieron terapia antimicrobiana inicial con cefalosporinas de 3ra generación (cefotaxime o ceftazidime). De 8 pacientes infectados, 6 fallecieron lo cual destaca la importancia de la detección de bacterias productoras de AmpC para asegurar una efectiva intervención terapéutica [12].
Métodos de detección fenotípica de betalactamasas AmpC
Como ya se mencionó no existen métodos fenotípicos estandarizados por el CLSI, para la detección de enzimas AmpC, no obstante, se han diseñado diversos procedimientos con elevada sensibilidad y especificidad.
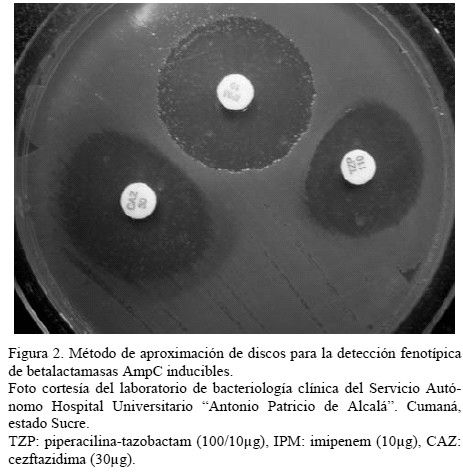
Método de aproximación de discos: Propuesto por Sanders y Sanders [24], es aplicable a betalactamasas AmpC inducibles. La técnica consiste en realizar un antibiograma convencional [25], para luego colocar un disco de cefoxitina o cualquier otro antimicrobiano inductor (Tabla 1) a una distancia de 27mm centro-centro de un disco de cefamandol, ceftazidima, ceftriazona o cefotaxima (antimicrobiano sustrato, revelador o testigo). El microorganismo producirá una betalactamasa inducible si se observa un halo de inhibición truncado del antimicrobiano sustrato, testigo o revelador [3, 26] (Fig. 2).
Tabla 1. Antimicrobianos inductores de la síntesis de betalactamasas cromosómicas inducibles
| Antimicrobianos con acción inductora elevada | Antimicrobianos con acción inductora débil |
| Benzil y aminopenicilinas | Ureidopenicilinas |
| Ácido clavulánico | Cefalosporinas de 3ra generación |
| Cefalosporinas de 1ra generación | |
| Cefoxitin | Cefalosporinas de 4ra generación |
| Imipenem | Aztreonam |
Tomado de Jacoby G [21].
Algunos autores han evaluado diversas combinaciones inductor-sustrato como: cefoxitina-piperacilina, imipenem-ceftazidima, imipenem-piperacilina/tazobactam e imipenem-cefoxitina; hallando que la combinación imipenem-piperacilina/tazobactam presenta la mayor sensibilidad y especificidad [27]. Ante una prueba positiva se debe alertar al clínico de la presencia de una betalactamasa inducible, que puede ocasionar un fracaso durante el tratamiento con betalactámicos para los cuales la AmpC es activa, como consecuencia de la selección de mutantes derreprimidos [1].
Detección de AmpC usando inhibidores específicos: El método de aproximación de discos no es de ninguna utilidad en cepas derreprimidas, hiperproductoras o con betalactamasas AmpC plasmídicas constitutivas. En estos
casos, deben adicionarse técnicas que incluyan la utilización de inhibidores de AmpC. La cloxacilina, constituye un inhibidor de AmpC cuya técnica consiste en inocular la cepa en estudio en placas con agar Mueller-Hinton según métodos convencionales, para luego colocar un disco de cloxacilina (500µg) y a ambos lados, discos de ceftazidima (30µg) y cefotaxima (30µg) a una distancia de 25mm centro-centro. Un aumento del halo de inhibición de las cefalosporinas adyacente a la cloxacilina, se interpreta como prueba positiva para la producción de AmpC [4]. Otros antimicrobianos como la oxacilina y el aztreonam, presentan de igual manera acción inhibitoria [21]. La detección de AmpC también puede llevarse a cabo utilizando ácido fenil borónico. Beesley y col., determinaron que el ácido fenil borónico (AFB), es un inhibidor competitivo reversible de las betalactamasas AmpC [6]. Uno de los métodos con AFB, consiste en utilizar discos de cefotetán (30µg) solos y suplementados con 20µl de una solución de AFB (400µg). Tras la realización de un antibiograma convencional, con los dos discos, se considera que existe una betalactamasa de tipo AmpC, si el halo de inhibición del disco con presencia de AFB es mayor o igual a 5 mm, en comparación con el halo del disco que no contiene este inhibidor. Esta técnica es conocida como potenciación de doble disco [28]. La preparación de la solución de ácido fenilborónico requiere dimetil sulfóxido (DMSO) como solvente, no obstante, debido a su toxicidad y poca accesibilidad en los laboratorios clínicos, se ha diseñado, recientemente, una técnica en donde se sustituye el DMSO por agua destilada, obteniendo los mismos resultados [29] (Tabla 2). La técnica de sinergia de doble disco también es otra sencilla opción para detección de AmpC usando AFB. Se basa en inocular una placa de agar Mueller-Hinton con la cepa a evaluar y colocar un disco de AFB (300µg). Seguidamente disponer a ambos lados de este, discos de cefotaxima (30µg) y ceftazidima (30µg) a una distancia centro-centro de 18mm. Después de la incubación, el observar una distorsión (expansión) del halo de inhibición de una o ambas cefalosporinas en las proximidades al disco de AFB, es indicativo de una prueba positiva (cepa productora de AmpC) [30].
Tabla 2. Preparación de soluciones de ácido fenilborónico para dispensar en discos a utilizar en la técnica de potenciación de doble disco.
| Técnica 1 (Referencias 28 y 30)
|
| Técnica 2 (Referencia 29)
|
Técnica con AFB en casos de coexistencia BLEE – AmpC: En aquellas cepas con producción conjunta de BLEE y AmpC, el AFB tiene una de las utilidades más notorias. La técnica confirmatoria de BLEE recomendada por el CLSI incluye la utilización de ácido clavulánico [31] y, tal como se mencionó al inicio del artículo, las AmpC resisten la inhibición por el clavulanato, por consiguiente, la presencia de BLEE puede ser enmascarada por la producción de AmpC [32]. La consecuencia de estos casos es el reporte de falsos negativos para BLEE. Song y col., modificaron la prueba confirmatoria de BLEE estandarizada por el CLSI. Esta técnica modificada consiste en añadir 20µl de una solución comercial de AFB (20g/l), a discos de cefotaxime (CTX) de 30µg (o ceftazidime de 30µg) y CTX con ácido clavulánico (10µg) (o ceftazidime-ácido clavulánico). Luego de inocular una placa con agar Mueller-Hinton según el método convencional, se coloca el disco de CTX+AFB y el de CTX-ácido clavulánico+AFB. Un incremento de 3mm o más en el diámetro del halo del disco de CTX+ácido clavulánico+AFB, en comparación con el disco de CTX+AFB, se considera una prueba positiva para BLEE [32]. El AFB inhibe la AmpC permitiendo determinar la presencia de BLEE. Derbyshire y col. desarrollaron una técnica similar con la finalidad de detectar coexistencia BLEE – AmpC, a través de la utilización de discos de cefepime y cefepime-ácido clavulánico [33].
Técnica de detección con discos AmpC, según Black y col.: Este método está basado en el uso de Tris-EDTA para permeabilizar la célula bacteriana y liberar las betalactamasas al medio externo. Los discos AmpC se preparan aplicando 20µl de una mezcla 1:1 de Tris-EDTA 100X y solución salina fisiológica estéril (SSFE), a discos de papel de filtro previamente esterilizados. Una vez preparados se dejan secar y se guardan en refrigeración hasta su uso. Seguidamente, se inocula una placa con agar Mueller-Hinton según el método de difusión con discos, con la
cepa ATCC 25922 de E. coli. Los discos preparados en el paso anterior, se rehidratan con 20µl de SSFE y se le aplican colonias de la cepa a estudiar. Posteriormente, se coloca un disco de cefoxitina (30µg) y, los discos AmpC ya inoculados, se ubican muy cercanos pero sin tocar el borde del disco de cefoxitina. La aparición de una distorsión de la zona de inhibición, indica inactivación de la cefoxitina por parte de la AmpC (AmpC +), y la ausencia de distorsión representa un resultado negativo (AmpC -). Esta técnica mostró un 100% de sensibilidad y 98% de especificidad [34]. Una prueba muy semejante, pero sin la adición de EDTA, es el método tridimensional descrito por Coudron [28].
Método fenotípico simple para la diferenciación entre AmpC cromosómicas y plasmídicas: Los diversos métodos fenotípicos mencionados no permiten diferenciar entre AmpC cromosómicas o plasmídicas (adquiridas). Mirelis y col., durante un estudio de rutina, observaron que aislados de E. coli, K. pneumoniae y P. mirabilis con un patrón de resistencia compatible con la producción de AmpC, mostraban un fenotipo diferencial en las placas de antibiograma. Este patrón consistió en la presencia de colonias dispersas localizadas dentro de los halos de inhibición de los discos de cefoxitina, cefotaxima, ceftazidima y aztreonam, cerca del borde de los mismos. Posteriormente, estudiaron por técnicas moleculares tres de los aislados, seleccionados al azar, encontrando que poseían la betalactamasa AmpC plasmídica CMY-2. En estudios subsiguientes, el patrón fenotípico de presencia de colonias dispersas dentro del halo arrojó 100% de sensibilidad y especificidad para la detección de AmpC plasmídicas [4]. El método resulta de particular utilidad en aquellas bacterias en las cuales es prácticamente imposible distinguir fenotípicamente entre una hiperproducción de AmpC cromosómica natural y una AmpC plasmídica debido a que ambas presentan el mismo patrón de resistencia. Sin embargo, esta diferencia es crítica para la vigilancia epidemiológica y el control de infecciones debido a que los genes mediados por plásmidos, pueden ser transferidos a otras especies bacterianas en el medio hospitalario y comunitario [13, 20].
Conclusiones
Es indiscutible la relevancia clínica de las betalactamasas AmpC, más aún, cuando se han encontrado mecanismos de resistencia asociados. Ejemplo: AmpC y pérdida de porinas, que amplían al rango de acción hidrolítica hasta los carbapenémicos; o las no menos preocupantes AmpC de espectro extendido que confieren resistencia a cefalosporinas de 4ta generación. Muchos laboratorios no determinan la presencia de AmpC debido, entre otras causas, a que se requieren reactivos no disponibles de manera rutinaria en el laboratorio clínico; no obstante, los métodos acá recopilados son accesibles y sencillos. Es importante recalcar que las enzimas AmpC (principalmente las plásmídicas), se asocian a fracasos terapéuticos, por lo que es importante su investigación empleando métodos para detección fenotípica y haciendo lectura interpretada del antibiograma. La resistencia a cefoxitín (a pesar de no ser 100% específica) en bacterias como K. pneumoniae, P. mirabilis o Salmonella spp., que no poseen naturalmente el gen AmpC, constituye un indicio de la presencia de betalactamasas AmpC plasmídicas con importancia epidemiológica por su potencial de diseminación. La detección también es importante para el monitoreo de bacterias con AmpC natural que durante el tratamiento con cefalosporinas se tornan resistentes, o en casos de cepas productoras de BLEE conjuntamente con AmpC. En cualquier caso, es esencial que los laboratorios clínicos microbiológicos incluyan como ensayo de rutina la detección fenotípica de betalactamasas tipo AmpC.
Referencias
1. Navarro F, Miró E, Mirelis B. Lectura interpretada del antibiograma de enterobacterias. Enferm Infecc Microbiol Clin. 2002; 20: 225-34. [ Links ]
2. Marín M, Gudiol F. Antibióticos betalactámicos. Enferm Infecc Microbiol Clin. 2003; 21: 42-55. [ Links ]
3. Perozo A, Castellano M. Pruebas de susceptibilidad a los agentes antimicrobianos. Maracaibo: Monografía. Sociedad Venezolana de Microbiología capítulo Zulia; 2005. [ Links ]
4. Mirelis B, Rivera A, Miró E, Mesa R, Navarro F, Coll P. A simple phenotypic method for differentiation between acquired and chromosomal AmpC β-lactamases in Escherichia coli. Enferm Infecc Microbiol Clin. 2006; 24: 370-2. [ Links ]
5. Bush K, Jacoby G, Medeiros A. A functional classification scheme for β-lactamases and its correlation with molecular structure. Antimicrob Agents Chemother. 1995; 39:1211-33. [ Links ]
6. Beesley T, Gascoyne N, Knott-Hunziker V, Petursson S, Waley S, Jaurin B et al. The inhibition of class C β-lactamases by boronic acids. Biochem J. 1983; 209: 229-33. [ Links ]
7. Juan C, Macía M, Gutiérrez O, Vidal C, Pérez J, Oliver A. Molecular mechanisms of β-lactam resistance mediated by AmpC hyperproduction in Pseudomonas aeruginosa clinical strains. Antimicrob Agents Chemother. 2005; 49: 4733-8. [ Links ]
8. Suárez C, Kattán J, Guzmán A, Villegas M. Mecanismos de resistencia a carbapenems en P. aeruginosa, Acinetobacter y Enterobacteriaceae y estrategias para su prevención y control. Infectio. 2006; 10: 85-93. [ Links ]
9. Vila J, Marco F. Lectura interpretada del antibiograma de bacilos Gram negativos no fermentadores. Enferm Infecc Microbiol Clin. 2002; 20: 304-12. [ Links ]
10. Bou G, Martínez J. Cloning, nucleotide sequencing, and analysis of the gene encoding an AmpC β-lactamase in Acinetobacter baumannii. Antimicrob Agents Chemother. 2000; 44: 428-32. [ Links ]
11. Schmidtke A, Hanson N. Model system to evaluate the effect of ampD mutations on AmpC- mediated β-lactam resistance. Antimicrob Agents Chemother. 2006;50: 2030-7. [ Links ]
12. Pai H, Kang C, Byeon K, Lee W, Park H, Kim E et al. Epidemiology and clinical features of bloodstream infections cause by AmpC-type-β-lactamases-producing Klebsiella pneumoniae. Antimicrob Agents Chemother. 2004; 48: 3720-8. [ Links ]
13. Pérez- Pérez FJ, Hanson ND. Deteccion of plasmid-mediated AmpC β-lactamases genes in clinical isolates by using multiplex PCR. J Clin Microbiol. 2002; 40: 2153-62. [ Links ]
14. Petrosino JF, Pendleton AR, Weiner JH, Rosenberg SM. Chromosomal system for studying AmpC-mediated β-lactam resistance mutation in Escherichia coli. Antimicrob Agents Chemother. 2002; 46: 1535-9. [ Links ]
15. Bush K, Macalintal C, Rasmussen B, Lee V, Yang Y. Kinetic interactions of tazobactam with beta-lactamases from all major structural classes. Antimicrob Agents Chemother. 1993; 37: 851-8. [ Links ]
16. Kazmierczak A, Cordin X, Duez J, Siebor E, Pechinot A, Sirot J. Differences between clavulanic acid and sulbactam in induction and inhibition of cephalosporinases in enterobacteria. J Int Med Res. 1990; 4: 67-77. [ Links ]
17. Livermore DM. Betalactamases in laboratory and clinical resistance. Clin Microbiol Rev. 1995; 8: 557-84. [ Links ]
18. Wolter DJ, Schmidtke AJ, Hanson ND, Lister PD. Increased expression of ampC in Pseudomonas aeruginosa mutants selected with ciprofloxacin. Antimicrob Agents Chemother. 2007; 51: 2997-3000. [ Links ]
19. Philippon A, Arlet G, Jacoby G. Plasmid-determined AmpC-type β-lactamases. Antimicrob Agents Chemother. 2002; 46: 1-11. [ Links ]
20. Cercenado E. Bacteriemia y colangitis por Escherichia coli productor de betalactamasas de tipo AmpC plasmídica. Madrid: Ediciones Francisco Soria Melguizo S.A.; 2008. [ Links ]
21. Jacoby G. AmpC β-Lactamases. Clin Microbiol Rev. 2009; 22: 161-82. [ Links ]
22. Bauernfeind A, Stemplinger I, Jungwirth R, Sahly H, Ullmann U. A novel type of AmpC β- lactamase ACC-1, produced by a Klebsiella pneumoniae strain causing nosocomial pneumonia. Antimicrob Agents Chemother. 1999; 43: 1924-31. [ Links ]
23. Reisbig M, Hossain A, Hanson D. Factors influencing gene expression and resistance for gram-negative organisms expressing plasmid-encoded ampC genes of Enterobacter origin. J Antimicrob Chemother. 2003; 51: 1141-51. [ Links ]
24. Sanders CC, Sanders WE. Emergence of resistance to cefamandole: posible role of cefoxitin inducible betalactamases. Antimicrob Agents Chemother. 1979; 15: 792-7. [ Links ]
25. Clinical and Laboratory Standards Institute (CLSI). Performance standards for antimicrobial disk susceptibility test; approved standard M2-A10. Wayne, Pennsylvania: CLSI; 2009. [ Links ]
26. Picazo JJ. Métodos especiales para el estudio de la sensibilidad a los antimicrobianos. España: Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica; 2000. [ Links ]
27. Dunne WH, Hardin DJ. Use of several inducer and substrate antibiotic combinations in a disk approximation assay format to screen for AmpC induction in patient isolates of Pseudomonas aeruginosa, Enterobacter spp., Citrobacter spp., y Serratia spp. J Clin Microbiol. 2005; 43: 5945- 9. [ Links ]
28. Coudron PE. Inhibitor-based methods for detection of plasmid- mediated AmpC β-lactamases in Klebsiella spp., Escherichia coli, and Proteus mirabilis. J Clin Microbiol. 2005; 43: 4163- 7. [ Links ]
29. Tenover F, Emery S, Spiegel C, Bradford P, Eells S, Endimiani A et al. Identification of plasmid- mediated AmpC β-lactamases in Escherichia coli, Klebsiella spp., and Proteus species can potentially improve reporting of cephalosporin susceptibility testing results. J Clin Microbiol. 2009; 47: 294- 9. [ Links ]
30. Yagi T, Wachino J, Kurokawa H, Susuki S, Kunikazu Y, Doi Y et al. Practical methods using boronic acid compounds for identification of class C β-lactamase- producing Klebsiella pneumoniae and Escherichia coli. J Clin Microbiol. 2005; 43: 2551- 8. [ Links ]
31. Clinical and Laboratory Standards Institute (CLSI). Performance standards for antimicrobial disk susceptibility testing; M100-S19. Wayne, Pennsylvania: CLSI; 2009. [ Links ]
32. Song W, Bae I, Lee Y, Lee C, Lee S, Jeong S. Detection of extended-spectrum β-lactamases by using boronic acid as AmpC β-lactamase inhibitor in clinical isolates of Klebsiella spp. and Escherichia coli. J Clin Microbiol. 2007; 45: 1180- 4. [ Links ]
33. Derbyshire H, Kay G, Evans K, Vaughan C, Kavuri U, Winstanley T. A simple disc diffusion method for detecting AmpC and extended-spectrum beta-lactamases in clinical isolates of Enterobacteriaceae. J Antimicrob Chemother. 2009; 63: 497-501. [ Links ]
34. Black J, Smith E, Thomson K. AmpC disk test for detection of plasmid mediated AmpC β-lactamases in Enterobacteriaceae lacking chromosomal AmpC β-lactamases. J Clin Microbiol. 2005; 43: 3110- 3. [ Links ]











 uBio
uBio