Introducción
La Organización Mundial de la Salud (OMS) define el síndrome metabólico como una condición patológica caracterizada por presentar obesidad, resistencia a la insulina, hipertensión e hiperlipidemia. Se estima que una cuarta parte de la población mundial la padecen 1, aumentando el ingreso hospitalario, contagio de COVID-19 2,3 y la muerte 4,5. Hasta el momento no existe un tratamiento para este síndrome, solo se controla y previene mediante un régimen dietético, actividad física y medicamentos; sin embargo, la población mexicana tiene poca adherencia a este 6,7 y debido al confinamiento ocasionado por el COVID-19 este se ha incrementado 8; además la ingesta constante de medicamentos, ocasiona efectos secundarios que afectan la calidad de vida del paciente 9,10,11,12,13,14,15,16,17,18,19,20, surgiendo el interés por tratamientos no farmacológicos mediante compuestos bioactivos 21,22. La OMS estima que el 80% de la población mundial utilizan extractos de plantas para tratar sus problemas de salud 23,24, entre las que destacan las especias 3,24 que presentan capacidad de disminuir la glucosa en sangre 25,26,27,28 y el colesterol total 29,30,31. La canela se consume en todo el mundo 3,32,33 y se utiliza en inflamación, náuseas, flatulencias, cólicos 34, fiebre, dolor de cabeza y amenorrea 35, además se le atribuyen múltiples propiedades biológicas 22,36 por los compuestos bioactivos que contiene entre los que destacan los polifenoles contenidos en un 90 % y el cinamaldehído entre un 60-75 %, otros constituyentes importantes incluyen el metileugenol, felandreno, benzaldehído, acetato de cinamilo, kaempferol, catequina, isorhamnetin, quercetina 23,37, ácido cinámico, alcohol de cinamilo y cumarina 38, además contiene vitaminas (A, B, K y C), minerales como: potasio, calcio, sodio, magnesio, manganeso, fósforo, colina, nitrógeno, cobre, hierro y zinc 39 y antioxidantes 40 que se pueden encontrar en forma volátil como: trasn-cinnamaldehido, cis-cinnamaldehído, eugenol, linalol, borneol, carvacrol, citral, limoneno, cimeno, safrol, alcohol cinnamílico, cariofileno, benzaldehído, pineno, acetato de L-bornilo y terpineol y en forma de fenoles como: ácido gálico, ácido vanílico, ácido clorogénico, ácido tánico, ácido cinámico, ácido sirínico, ácido sinapico, ácido cafeico, ácido cumarico, ácido p-hidroxibenzoico, p-hidroxibenzaldehído y ácido ferúlico 41, además de altos niveles de diferentes compuestos fitoquímicos con acciones captadoras de radicales libres, como: epicatequina, canfeno, gamma-terpineno, fenol, ácido salicílico, taninos, proantocianidinas, oligómeros de las catequinas y epicatequina. Por lo que esta revisión tiene como objetivo documentar los estudios in vitro, in vivo, clínicos y los mecanismos de acción reportados del efecto de la administración de canela en las comorbilidades relacionadas con el Síndrome Metabólico.
Materiales y métodos
Se realizó una revisión sistemática en base a la metodología "PRISMA" 42, la cual comenzó con la búsqueda de artículos en las siguientes bases de datos: PubMed, Science Direct y Google Scholar, mediante las siguientes palabras clave: "Cinnamomum", "hipertensión", "diabetes", "obesidad" y "dislipidemia", en un período desde Julio a Octubre de 2020, realizando una búsqueda inicial que consistió en la lectura de los titulos y abstracts, si parecían tener relación con el tema en cuestión se descargaban en pdf, obteniendo un total de 123 artículos, a los cuales se les aplicaron los siguientes criterios de inclusión para su selección:
a)Artículos originales de Open Access, b) Publicados de 2015 a 2020, c) Artículos publicados en inglés y d) Artículos que incluyeran al menos un grupo control y como criterios de exclusión se establecieron los siguientes: a) Artículos relacionados con su efecto antimicrobiano, antifúngico y aceite de canela, b) Artículos sin el archivo pdf disponible, c) Artículos publicados fuera del rango establecido (2015-2020) y d) Artículos de revisión.
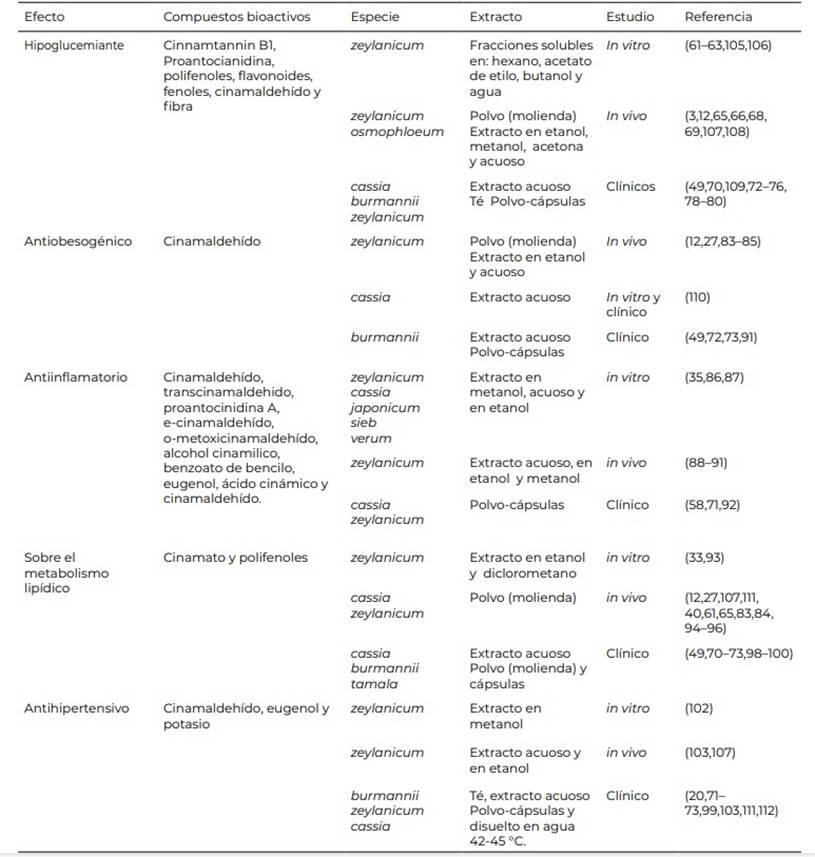
De esta forma se obtuvieron un total de 60 artículos, de los cuales 13 corresponden a estudios in vitro, 25 in vivo, 20 clínicos y 2 investigaciones realizadas con modelos tanto in vitro como in vivo, los cuales se presentan en la Tabla 1, indicando el tipo de estudio (in vitro, in vivo o estudio clínico), la forma en que utilizaron la canela (extracto, polvo obtenido con molienda, cápsulas, té o fracciones del mismo), la especie y los compuestos bioactivos que en el artículo consideran que son responsables del efecto relacionado a las comorbilidades del síndrome metabólico.
Resultados
Características generales de la canela
La canela es una especia obtenida de la corteza seca de los árboles del género Cinnamomum 43 el cual se compone de aproximadamente 250 especies 44, comprendiendo cuatro especies principales zeylanicum, burmanni, saigon y cassia 32,45,46. Proporciona proteínas, fibra, componentes volátiles, vitaminas (A, B, K y C), minerales como potasio, calcio, sodio, magnesio, manganeso, fósforo, colina, nitrógeno, cobre, hierro y zinc 39. Contiene antioxidantes como fenoles, glucósidos y taninos 47, además de compuestos bioactivos a los cuales se les han comprobado los siguientes efectos en la salud humana: aumento del flujo sanguíneo, antimutagénico, antitumoral, hipoglucemiante, antilipemiante, antimicrobiano, diarrea, flatulencias, asma, bronquitis, infecciones, regeneración de tejidos, antiinflamatoria, hepatoprotectora y pérdida de peso 32,48,57,58,49,50,51,52,53,54,55,56. La Administración de Drogas y Alimentos de los Estados Unidos declaró que la canela es considerada como segura (GRAS). Además, estudios realizados sobre su toxicidad 41,59,60 indican que es un ingrediente seguro para usar en alimentos y está permitido como conservante en la mayoría de los países con efectos protectores contra toxinas naturales y químicas.
Efecto hipoglucemiante
La canela ha comprobado la reducción de hiperglucemia post prandial in vitro causada principalmente por la gran cantidad de antioxidantes que contiene 61 que producen actividad de anti amilasa moderada 62, como las proantocinidinas y taninos que disminuyen la resistencia a la insulina y leptina 63, mientras que el aldehído cinámico y eugenol inhiben la enzima α glucosidasa 64. En estudios in vivo el extracto etanólico de Cinnamomum zeylanicum redujo 11.6 % el nivel de glucosa y aumentó 7,2 % el nivel de insulina en ratas, atribuyendo este afecto a la acción del trans-cinamaldehido presente en la canela 3. En inducción de diabetes con estreptozotocina (STZ) 65,66 y aloxano 12,67 el extracto etanólico de Cinnamomum zeylanicum y extracto de Cinnamomum osmophloeum disminuyeron el nivel de glucosa en sangre y hemoglobina glucosilada, ocasionado por las proantocinidinas tipo A, también se reporta la restauración del tejido renal y pancreáticocon extracto metanólico de canela 68. En diabetes gestacional el cinamaldehído aumentó la secreción y sensibilidad de la insulina 69. Los estudios clínicos reportan disminución significativa de glucosa pospandrial y hemoglobina glicosilada tanto en pacientes sanos, como prediabéticos y diabéticos con dosis de 500 mg de extracto acuoso, 1,5 y 3 g de polvo en cápsulas al día70,71,72,73,74,75,76,77. Estudios adicionales reportan eficacia con ingesta de 0.5 g y 1 g de canela en polvo durante 3 meses en pacientes con DT2 (Diabetes Tipo 2) mal controlados 78,79 y pacientes con obesidad 49, atribuyendo este efecto a los antioxidantes 76,78,79,80, catequinas y epicatequina(81) y cinamaldehído 74.
Efecto antiobesogénico
La canela demuestra con ensayos in vitro un aumento en el gasto de energía a través de las células musculares 82, en estudios in vivo se han determinado factores genéticos asociados con la obesidad a través de la disminución de sus características genotípicas y fenotípicas, como la investigación realizada por Navrinder et al. quien evaluó estos parámetros en pez cebra, encontrando la disminución del peso corporal e índice de masa corporal (IMC) atribuyendo este efecto a la presencia de polifenoles 83. Mientras que en modelos in vivo realizados en ratas, autores como Lopes et al. sugieren que el extracto acuoso de canela atenuó el proceso lipogénico a través de la regulación de la expresión de factores transcripcionales y genes involucrados en la lipogénesis 84, mientras queautores como Kwan et al. refieren que el ácido protocatecúico, catequina, ácido clorogénico, esculetina, quercetina e icariinal contenidas en el extracto etanólico de canela Cinnamomum cassia induce el adipocito marrón, con lo que se reduce el peso corporal 85, caso similar al reportado por Song et al., quien además encontraron que posiblemente el cinamaldehído ocasionó la disminución en el tamaño de los adipocitos y aumento de la masa muscular en ratones obesos 82, presentándose también en ratas hipotiroideas 27 y con diabetes 12. Los estudios clínicos reportados incluyen cambios en la circunferencia de cintura y peso corporal 72, además de reducción en el IMC, relación cintura-cadera y adiposidad abdominal 49,73, efecto reportado también en pacientes con Diabetes tipo 2 (DT2) 18, donde además se observó aumento en la masa magra, siendo responsable de estos efectos los antioxidantes contenidos en la canela 12,81.
Efecto antiinflamatorio
La actividad antiinflamatoria de la canela se ha informado en algunos estudios in vitro identificando diferentes compuestos bioactivos responsables, como al ácido cinámico, cinamaldehído 86, E-cinamaldehído, o-metoxicinamaldehído 35, trans-cinamaldehído y p-cimeno 87. Mientras que los estudios in vivo realizados en ratas reportan disminución en la expresión de diversos mediadores proinflamatorios 88, tras la inducción de una neurotoxicidad con formaldehído 89 y de un daño con acrilamida. Autores como Haidari et al. observaron reparación de lesión hepática, mientras que en presencia de dieta alta en fructosa y sobrepeso 90, mientras que Sohrabi et al. reportaron disminución de las condiciones inflamatorias 91. Min Seo et al. sugieren que la canela podría atenuar la inflamación intestinal 86. Estudios clínicos recientes demuestran reducción significativa de la inflamación en pacientes con DT2 71 y reducción de gravedad y duración de migraña 92.
Efectos sobre el metabolismo lipídico
Existen pocos estudios in vitro reportados recientemente de la acción hipolipemiante de la canela, debido a que este efecto ya ha sido comprobado mediante la acción de las enzimas 3-hidroxi-3-metilglutaril-coenzima A (HMG-CoA), reductasa, lipasa, colesterol esterasa y de la micelización del colesterol por el cinamaldehido 33. Hoy et al. identifica los compuestos cinamiloiso butirato y cinnamaldehído como los responsables de la reducción de triglicéridos (TG) y fosfolípidos (PL) 93. La mayoría de los estudios in vivo reportados coinciden que tras la suplementación con canela mejoran los parámetros bioquímicos de los lípidos, a través de la disminución significativa en los niveles de colesterol y triglicéridos en plasma 84,94 presentándose tanto con inducción de diabetes con aloxano 12, como con esprectrozotocina, donde además se presentó disminución en lipoproteínas de muy baja densidad (VLDL) 61 y aumento en las lipoproteínas de alta densidad (HDL) 65,95, además de disminución en la aparición de hígado graso 96. Diversos autores atribuyen estos efectos al aumento de expresión de genes relacionados con el metabolismo de los lípidos 22,83,97. Debido al efecto antihiperlipemiante y seguridad hepática comprobados, se han realizado varios estudios clínicos, observando los mismos resultados de disminución en los niveles de colesterol total, LDL, TG y el aumento de HDL en suero de forma significativa 70,73,98 en pacientes con sobrepeso y obesidad (49), mujeres con síndrome de ovarios poliquísticos 99, pacientes con DT2 72,74 y pacientes con hipertensión grado 1 100. Autores como Nayak et al. identifican al compuesto cinamaldehído como el responsable de los efectos hipolipidémicos asociados con el aumento en los niveles de adiponectina 101.
Efecto antihipertensivo
El estudio in vitro de Ranjini et al. reportan que posiblemente el cinamaldehído y cinamato inhibieron significativamente la enzima convertidora de angiotensina 102, similar a la disminución que se obtiene al tomar el fármaco captopril; con lo que se promueve su uso en el control de la presión arterial y reducción de enfermedades cardiovasculares con menores efectos secundarios relacionados a los fármacos antihipertensivos 17,18,19,20. Los estudios in vivo reportados por Sedighi et al. así como la reducción de infarto al miocardio, a través de la mejora en la lesión miocárdica inducida por isquemia mediante extracto de Cinnamomum zeylanicum 103, así como el aumento en el grosor de la aorta encontrada por Nayak et al. efectos que se le atribuyen a la presencia de ácido cinámico, metileugenol y cinamaldehído 101. Con lo que se comprueba el potencial de la canela en la reversión de daño cardíaco y aterogénico. Los estudios clínicos reportados revelan la disminución significativa en la presión arterial 72,91 en mujeres con hipertensión 104, pacientes con síndrome metabólico 73 y DT2 74.
Mecanismos de acción
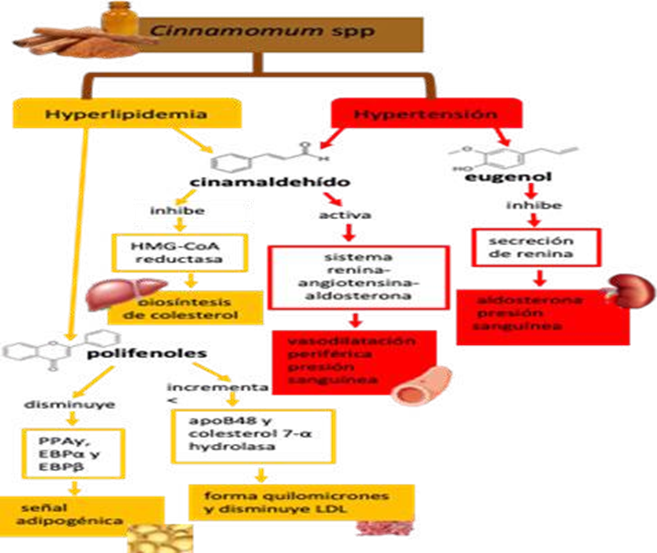
De los 60 artículos consultados, 29 de ellos sugieren diferentes mecanismos de acción a través de los cuales los compuestos bioactivos de la canela median sus efectos en las comorbilidades relacionadas con el síndrome metabólico: diabetes, obesidad e inflamaciónlos cuales se representan en la Figura 1 e hiperlipemiante y antihipertensivo en la Figura 2. En ambas figuras se observa que el compuesto cinamaldehído interviene en las cinco condiciones, presentando actividad hipoglucemiante al activar la enzima quinasa, permitiendo la unión de la insulina a las células, así como la inhibición de la enzima fosfatasa, conduciendo a una fosforilación de la glucosa 5,48 y a la regulación del ácido ribonucleico mensajero (ARNm) del receptor gamma activado por el proliferador de peroxisomas (PPARg) mejorando la sensibilidad a la insulina 49. Con efecto antiobesogénico estimula el tejido adiposo pardo interescapular, aumentando el termogénico (UCP1) y proteína visceral que disminuye la distribución de grasa corporal (50). En inflamación suprime la enzima óxido nítrico sintasa (NOS) que relaja el músculo liso de la pared vascular e inhibe la adhesión de plaquetas provocando una disminución de la inflamación; y la enzima ciclooxigenasa (COX) inhibe la formación de sustancias inflamatorias 51,52. Como hipolipemiante inhibe la enzima HMG-CoA reductasa deteniendo la biosíntesis de colesterol en el hígado, suprimiendo la peroxidación lipídica 34,46,53,54 y tiene efecto sobre hipertensión al activar la enzima convertidora de angiotensina (ECA) que promueve las reacciones del sistema renina-angiotensina-aldosterona que inducen la dilatación de los vasos periféricos disminuyendo la presión arterial 55-57.
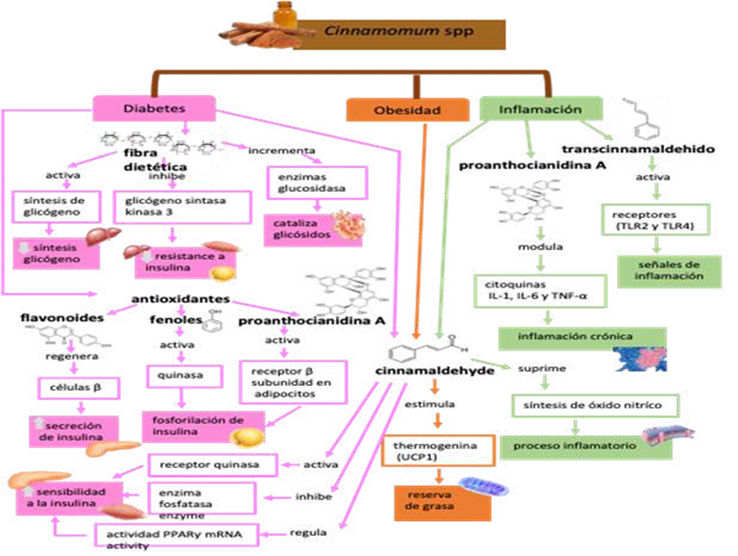
Figura 1 Mecanismos de acción de los compuestos bioactivos de la canela en las comorbilidades de diabetes, obesidad e inflamación. (Autoría propia)
Conclusiones
Este artículo de revisión recaba evidencias de investigaciones reportadas en modelos in vivo, in vitro y casos clínicos de canela, validando su potencial en el tratamiento de enfermedades relacionadas al síndrome metabólico, debido a sus principales compuestos bioactivos: cinamaldehído, transcinamaldehído, ácido cinámico, eugenol, y antioxidantes del tipo proantocianidinas A y flavonoides, los cuales participan en diversos mecanismos de acción que activan e inhiben enzimas con efecto hipoglucemiante(quinasa y fosfatasa), antiobesogénico (UPC1), antiinflamatorio (NOS y COX), hipolipemiante (HMG-CoA) y antihipertensivo (ECA), con lo que mejora la sensibilidad a la insulina, disminuye grasa corporal, disminuye e inhibe la formación de sustancias inflamatorias, suprime síntesis de colesterol e induce la dilatación sanguínea. Por lo que la canela demuestra su uso potencial como coadyuvante en el tratamiento de las comorbilidades del síndrome metabólico.